Аннотация
Аутологичная клеточная терапия — увлекательное направление в медицине против старения. Широкий спектр продуктов: обогащенная тромбоцитами плазма, фибрин, трансплантаты жировой ткани в виде микронизированных жировых трансплантатов (микрожир) или гомогенизированного геля (нанофат), а также стромально-васкулярная фракция позволяют проводить индивидуализированное лечение пациентов, стремящихся к интенсивному омоложению, а также объему. Биопрепараты – мощная альтернатива филлерам и биостимуляторам. Средства их воздействия на кожу намного превосходят то, что синтетические продукты позволяют достичь инъекторам. Основным показанием для обогащенной тромбоцитами плазмы является омоложение и коррекция морщин. Он также часто используется в комбинированной терапии алопеции, рубцов, хронических ран, гиперпигментации и акне. Активные тромбоциты выделяют множество факторов роста, цитокинов, сильно влияющих на восстановление тканей. Пересадка жира может быть выполнена за одно посещение благодаря новым системам, которые позволяют перерабатывать жировую ткань без необходимости лабораторной подготовки. Жировая ткань является самым большим эндокринным органом, переносчики жира состоят из множества активных клеток. Его биологическое воздействие на ткани заключается в сильном омоложении и восстановлении поврежденной кожи. Доступная литература по липофилингу и использованию стволовых клеток по эстетическим показаниям более обширна. Будущие тенденции включают улучшение приживаемости жировых трансплантатов различными способами, такими как введение факторов роста.
Растущая популярность аутологичных производных продуктов наблюдается не только в спортивной и регенеративной медицине, но и в антивозрастной медицине. Основным преимуществом использования биологических агентов является их природный источник. Пациенты, решившиеся на лечение аутологичными методами, стремятся добиться естественного, омолаживающего результата. Широкий спектр аутологичных продуктов позволяет проводить индивидуальное лечение, отвечающее ожиданиям широкого круга пациентов. Среди продуктов аутологичного происхождения можно выделить богатую тромбоцитами плазму, фибрин, трансплантаты жировой ткани в виде микронизированного жирового трансплантата (микрожир) или гомогенизированного геля (нанофат), а также стромально-васкулярную фракцию (разговорный источник стволовых клеток, СВФ). Используемые в настоящее время методики не требуют многочасовой лабораторной подготовки и могут быть выполнены сразу за одну процедуру.
Аутологичная кондиционированная плазма
Аутологичная кондиционированная плазма (ACP) или богатая тромбоцитами плазма (PRP) является популярным методом лечения. Основными показаниями для ACP в эстетике являются омоложение и коррекция морщин.
лечение алопеции, рубцов, хронических ран, гиперпигментации и акне. При применении после абляционных процедур или операций ускоряет заживление ран и выздоровление. Наиболее сильными агентами при АКП являются активные тромбоциты. Стимулируя фибробласты, они индуцируют секрецию коллагена, эластина, металлопротеиназ (ММП) и самосинтез гиалуроновой кислоты. Альфа-гранулы отвечают за высвобождение факторов роста и цитокинов. PDGF (тромбоцитарные факторы роста) являются хемотаксическими агентами для фибробластов и макрофагов, TGF-B (трансформирующий фактор роста), EGF (эпидермальный фактор роста) и VEGF (фактор роста эндотелия сосудов). ) опосредуют ангиогенез, тогда как FGF (фактор роста фибробластов) стимулирует пролиферацию клеток и фибробластов. D-гранулы секретируют серотонин и АДФ.
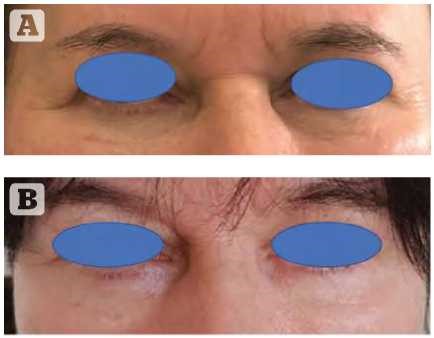
ACP рекомендуется применять в течение нескольких процедур. В большинстве случаев это три процедуры, проводимые каждые 4 недели. После серии процедур должно быть заметно улучшение состояния кожи. Несколько исследований показали уменьшение морщин, улучшение натяжения и эластичности кожи, уменьшение гиперпигментации и умеренный объем, что было вторичным по отношению к подтяжке и укреплению кожи. Этот эффект также может быть результатом способности стимулировать собственную секрецию гиалуроновой кислоты (ГК) и повышенной секреции коллагена типа I. Общие показания включают меланоцитоз нижнего века и кожи, который, как известно, улучшается при лечении АСР. После серии процедур видно улучшение плотности кожи и коррекция мелких морщин (рис. I). В случае алопеции EGF и TGF играют наиболее важную роль, способствуя созреванию волосяных фолликулов. Другие агенты также ингибируют клеточный апоптоз. АКП успешно используется в монотерапии, но при сочетании с другими методами спектр возможностей расширяется. Комбинированная терапия включает лечение посттравматических рубцов, когда АКП предшествуют абляционные лазеры или радиочастоты с микронидлингом, или шрамов от угревой сыпи, когда возможно использование поверхностных пилингов в одном протоколе с АКП и микронидлингом, а АКП является безопасным и эффективным лечением. Известно, что могут возникать такие эффекты, как покраснение, отек, кровоподтеки, боль и ощущение жжения или зуда, но до сих пор не сообщалось о серьезных побочных эффектах.
Продукты жирового происхождения
Жировую ткань часто называют «Золушкой анатома», так как на протяжении многих десятилетий ею пренебрегали, а ее роль сводилась к хранению энергии, липогенезу и липогенолизу. Между тем, он чрезвычайно метаболически и гормонально активен. Жировая ткань является крупнейшим эндокринным органом, а адипоциты выделяют сотни факторов роста и гормонов.
На поверхности мембран адипоцитов также имеется множество рецепторов, регулирующих их активность, таких как рецепторы инсулиноподобных факторов роста (IGFR-1 и 2), цитокинов, тиреоидных гормонов и витамина D. Адипоциты имеют на своей поверхности рецепторы CXCR4, которые известно, что это путь передачи ВИЧ, но он также отвечает за липодистрофию у больных СПИДом и при болезни Крона. Адипоциты играют чрезвычайно важную роль в цикле роста волос. При этом 10% зрелых адипоцитов подкожной клетчатки ежегодно претерпевают цикл преобразований, аналогичный кератиноцитам. В экстремальных условиях, таких как голодание или шок, часть подкожной белой жировой ткани трансформируется в бурую жировую ткань (эффект подрумянивания) и защищает систему гомеостаза и терморегуляции.
Жировая ткань стареет. С возрастом увеличивается количество макрофагов М2 и снижается количество макрофагов М1, что ухудшает нейтрализацию свободных жирных кислот и приводит к развитию атеросклероза и увеличению массы тела. Со временем способность к пролиферации и секреции адипонектина также снижается, а секреция провоспалительных цитокинов увеличивается. Это может быть причиной того, что время выживания жировых трансплантатов все еще непредсказуемо, и у пожилых пациентов конечный результат может быть менее удовлетворительным, чем у более молодых пациентов. Конечный результат сильно зависит от пациента, и менее благоприятные результаты липофилинга у пожилых пациентов могут быть связаны не с плохой техникой, а со старением жировой ткани.
Физиология
Помимо адипоцитов, которые составляют 90% объема ткани, жировая ткань содержит множество других активных клеток. Наиболее известными клетками являются мезенхимальные стволовые клетки жирового происхождения (МСК). Это мультипотентные клетки; однако in vivo они не размножаются, а вместо этого действуют как регуляторные клетки. При попадании в поврежденную ткань они стимулируют регенерацию тканей за счет секреции факторов роста фибробластов, эндотелия и противовоспалительных цитокинов. В результате образуются коллаген, эластин и другие белки внеклеточного матрикса. Моделирование мягких тканей происходит за счет металлопротеиназ. Неоваскуляризации способствуют в основном перициты. Это также мультипотентные клетки, которые in vivo не пролиферируют в адипоциты или фибробласты, но координируют регенерацию поврежденных тканей. Паракринный диалог между активными клетками жировой ткани управляется иммунными клетками. Они также предотвращают инфекцию за счет презентации антигена и гуморальных или клеточных ответов. Жировая ткань является не только средством для увеличения объема, но и источником сильной и глубокой регенерации тканей благодаря наличию стволовых клеток, перицитов и адипоцитов. Именно это делает жировую ткань отличной альтернативой другим наполнителям мягких тканей.
Жировая ткань характеризуется низким риском отторжения и аллергии. Сбор жировой ткани возможен в большинстве случаев. Средняя приживаемость трансплантатов варьируется от 10% до 90%. Вот почему непредсказуемые показатели выживаемости считаются главным недостатком аутологичной пересадки жира. В раннем посттрансплантационном периоде молекулы жира питаются за счет осмоса. В соответствии с принципом Йошимуры частицы жира размером менее 200 микрон наименее подвержены апоптозу. При переносе мелких частиц жира также уменьшается риск образования комков. Большинство доступных на рынке наборов для пересадки жира предлагают устройства для сбора и гомогенизации жира, которые обеспечивают высочайшее качество жировой ткани. Кроме того, добавление АСР или стволовых клеток, полученных из стромально-васкулярной фракции (липотрансфер с помощью CAL-клеток), стимулирует процесс неоваскуляризации.
Использование продуктов, полученных из жировой ткани
Использование жировой ткани в качестве наполнителя мягких тканей имеет давнюю традицию: первая липотрансплантация была проведена в 1893 году Адольфом Нойбером. Потребовалось еще сто лет, чтобы идентифицировать стволовые клетки, полученные из жировой ткани. Подкожная жировая ткань является идеальным источником стволовых клеток. Из подкожного жира можно получить в 500 раз больше стволовых клеток, чем из костного мозга. Наиболее распространенные показания к пересадке жира и стромально-васкулярной фракции:
- Беременность и лактация
- Активные опухолевые процессы
- Активные инфекции
- Активные аутоиммунные заболевания
- Расстройства коагуляции
- Тромбоз
- Недостаточное количество подкожной жировой ткани
Жировая ткань является крупнейшим эндокринным органом, а адипоциты выделяют сотни факторов роста и гормонов.
Противопоказания для аутологичной клеточной терапии:
- Объемметрия
- Лечение дефицита мягких тканей, в том числе после РТГ
- Регенерация и омоложение
- Коррекция тонких линий
- Лечение алопеции
- Комбинированное лечение ссар, в том числе рубцов от прыщей посттравматического и гипертрофического
- Лечение перианальных свищей
- Лечение хронических ран
Однозначных отчетов или руководств по аутологичной клеточной терапии у онкологических больных нет. Известно, что мезенхимальные стволовые клетки не пролиферируют in vivo и не подвергаются неопластической трансформации. Однако мезенхимальные стволовые клетки стимулируют ангиогенез; следовательно, риск стимуляции неопластической сосудистой сети и метастазирования представляется очень высоким. Одно исследование выявило улучшение заживления и более длительный период ремиссии при плоскоклеточном раке головы и шеи после заполнения дефектов мягких тканей аутологичными агентами. С другой стороны, есть исследования, показывающие локальное прогрессирование протоковой аденокарциномы в молочной железе и ускоренное образование отдаленных метастазов. При эстетических показаниях крайне важно собрать у пациента надлежащий анамнез и тщательно изучить его перед процедурой.
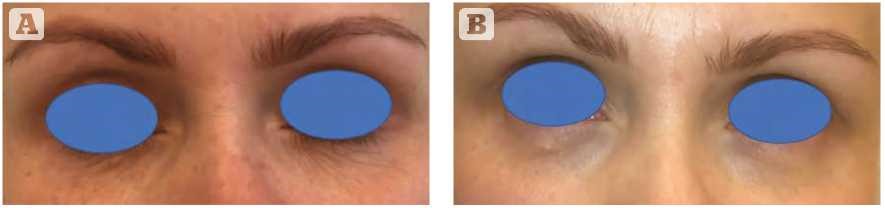
Идеальным кандидатом на пересадку жировой ткани будет пациент, которому требуется большой объем восстановления, а также сильное омоложение и регенерация кожи, при этом подкожная жировая ткань на донорском участке может быть взята. неудачные филлеры на основе гиалуроновой кислоты в области нижнего века и разрыв В опытных руках пересадка жира сопряжена с меньшим риском образования комков и гиперкоррекции, чем гиалуроновая кислота. Сильная регенерация и подтяжка кожи, а также улучшение дермального меланоцитоза в области нижнего века могут быть усилены, а удовлетворительные долгосрочные результаты могут быть достигнуты путем добавления мезенхимальных стволовых клеток к жировому трансплантату. На рис. 2 представлен случай выраженного омоложения нижнего века после пересадки 1,5 мл гомогенизированного жирового трансплантата (наножира), покрытого стромально-васкулярной тракцией по 1 мл на участок. Видно улучшение объема, а также коррекция тонких линий, повышение тонуса и эластичности кожи.
Профиль безопасности
Эффекты от использования жировой ткани, несмотря на большой объем, очень естественны. Однако следует помнить, что это более инвазивные процедуры с риском осложнений и длительным обучением оператора. Согласно ограничениям FDA, аутологичные продукты, разрешенные для использования в эстетической медицине, не должны подвергаться манипуляциям, не должны сочетаться с внешними агентами, а также должны быть однородными и использоваться в одной и той же процедуре. Наиболее распространенным побочным эффектом является отек, который может сохраняться до месяца после процедуры. В литературе описаны случаи миграции трансплантата, образования кальцинатов и кист, а также ишемии, некроза, потери зрения. Следует соблюдать крайнюю осторожность при введении жировой ткани с тщательной оценкой анатомии пациента и использованием канюль. Рекомендуется вводить слегка перекорректированные отложения, так как часть трансплантата будет рассасываться. Осложнения также могут быть связаны с процессом извлечения ткани. Не следует забывать и о риске жировой эмболии и тромботических осложнений.

Методы безопасной и эффективной пересадки жира все еще находятся на стадии разработки. Недавно обсуждались некоторые будущие тенденции. Аллогенная пересадка жира также кажется интересной альтернативой; однако иммуногенность жировой ткани может оказаться серьезной проблемой. Предпринимаются усилия по разработке различных каркасов и факторов роста, которые можно было бы безопасно добавлять к жировым трансплантатам для улучшения их выживаемости. Наконец, есть наблюдения, что простые методы, такие как ботулин, могут иметь благотворное влияние на результаты липофилинга. Расслабляя подвижные части лица перед переносом жира, механическое напряжение мышц уменьшается, и считается, что частицы жира сохраняются дольше.
Одной из самых многообещающих инноваций в биологической очистке может быть криоконсервация. Жир, удаленный во время плановой липосакции, можно заморозить, сохранить и использовать в случае необходимости и в течение нескольких лет.
Выводы
Растущий интерес врачей и пациентов к аутологичной клеточной терапии в антивозрастной медицине привел к увеличению количества сообщений и спроса на лечение. Это направление, которое динамично развивается и с каждым годом появляются улучшения. Биопрепараты – мощная альтернатива филлерам и биостимуляторам. Способы их воздействия на кожу далеко превосходят возможности синтетических продуктов и к тому же чрезвычайно увлекательны.
Аутологичная клеточная терапия для омоложения лица набирает популярность
Активные тромбоциты, полученные с помощью обогащенной тромбоцитами плазмы (PRP), активируют ремоделирование внеклеточного матрикса, секрецию аутологичной гиалуроновой кислоты, коллагена и эластина.
Стволовые клетки представляют собой мультипотентные клетки, которые индуцируют регенерацию тканей, но не размножаются in vivo.
С помощью липотрансфера можно добиться восстановления объема, а также омоложения и улучшения качества кожи.
Одной из самых многообещающих инноваций в биологической очистке может быть криоконсервация. Жир, удаленный во время плановой липосакции, можно заморозить, сохранить и использовать по требованию в течение нескольких лет.
